In questi giorni ci sentiamo vacillare, bombardati da notizie sull’emergenza sanitaria e preoccupati per il nostro futuro.
Cerchiamo informazioni per capire cosa stia succedendo e cosa succederà, ma purtroppo spesso queste informazioni ci mandano ancor di più in confusione perché sono in contrasto tra loro o perché non abbiamo gli strumenti adatti per capirle fino in fondo. Questo avviene in particolare quando scienza, politica e economia si sovrappongono in una situazione di interesse internazionale come quella che stiamo vivendo.
Noi, da bravi appassionati di scienza, ci affidiamo alla biologia e stavolta chiediamo aiuto ad un Biologo che ha avuto a che fare proprio con i Coronavirus: Antonello Pelosi, laureato in Ecobiologia all’Università Sapienza di Roma e con un master in Genetica Forense, dopo un secondo master in Virologia Molecolare ha contribuito ad un lavoro pubblicato nel 2016 sulla Sindrome Respiratoria Medio Orientale da Coronavirus (MERS) - The global spread of Middle East respiratory syndrome: an analysis fusing traditional epidemiological tracing and molecular phylodynamics1.
Quali sono le analogie e le differenze a livello morfologico ed epidemiologico tra il nuovo coronavirus SARS-CoV2 e i già conosciuti coronavirus SARS-CoV e MERS-CoV?
I Coronavirus di interesse umano degli ultimi 18 anni, SARS-CoV (diffusione di SARS nel 2002), MERS-CoV (diffusione di MERS nel 2012) e SARS-CoV-2 (attuale diffusione di Covid-19), rientrano tutti nel genere dei Betacoronavirus: condividono la maggior parte del materiale genetico ed esprimono strutturalmente più o meno le stesse componenti virali2.
Alcune di queste rimangono maggiormente conservate durante il corso dell’evoluzione, mentre altre sono molto variabili e predisposte a cambiare nel corso del tempo3. È questo il caso del gene S che codifica la proteina virale Spike, coinvolta nell’interazione con i nostri recettori cellulari al momento dell’infezione.
Spike può variare nei diversi coronavirus per infettare le cellule del tessuto polmonare mediante target differenti: durante il processo di infezione sia SARS-CoV sia SARS-CoV-2 utilizzano Spike per legare un certo tipo di recettori cellulari (chiamati ACE2), mentre MERS-CoV utilizza una variabile di Spike per legare un altro tipo di recettori cellulari (chiamati DPPR). Conoscere la genetica, la diversità d’espressione delle proteine virali, le vie d’ingresso nella cellula e come la cellula risponde a tale attacco, è utile per mettere a punto cure e terapie antivirali specifiche4.
Per quanto riguarda l’epidemiologia ad oggi si sa ben poco. In alcuni tamponi la carica virale, ossia la quantità di particelle virali, dell’attuale SARS-CoV-2 è stata stimata essere fino a 1.000 volte maggiore rispetto a quella del SARS-CoV. Sicuramente si parla di un modello di maggiore contagiosità del SARS-CoV-2 rispetto al SARS-CoV e questo è quotidianamente sotto gli occhi di ognuno di noi. SARS-CoV ha infettato circa 8.000 persone in tutto il mondo in 8 mesi, mentre ad oggi SARS-CoV-2 ha infettato oltre 1 milione di persone in 3 mesi (03/04/2020), con un dato decisamente in crescita viste le ultime notizie preoccupanti in arrivo da Europa, USA, IRAN. Questi dati sono ovviamente sottostimati perché, come sappiamo tutti, lo screening mediante tampone viene fatto solo a chi ha già i sintomi da Covid-19 e questo non descrive realmente il fenomeno. In realtà il numero è ipoteticamente maggiore e fortunatamente questo ne abbassa notevolmente il tasso di letalità. Infatti a livello globale il tasso di letalità (con i dati sottostimati attualmente a disposizione) è intorno al 5% (03/04/2020), mentre si attesta intorno al 10 % per SARS-CoV e del 35% per MERS-CoV5, 6.
Sicuramente con il tempo avremo un quadro maggiormente realistico del fenomeno.
Sulla base delle conoscenze scientifiche è possibile prevedere la durata dell’attuale pandemia?
L’andamento tipico di un’epidemia viene descritto da una curva a forma di “S” allungata (denominata sigmoide), generalmente caratterizzata da 3 fasi.
Fase “esponenziale”: il numero degli individui contagiati aumenta progressivamente giorno per giorno.
Fase “logistica”: i contagi aumentano, ma più lentamente e quantitativamente meno rispetto alla prima fase.
Tra queste prime due fasi c’è un punto di flesso della curva che porta ad una fase stazionaria. In questo momento la curva si satura, i contagi diminuiscono rispetto alle precedenti fasi e giorno per giorno si hanno mediamente gli stessi numeri di contagiati.
Fase di “decrescita”: i contagi diminuiscono giorno per giorno fino ad avere una diminuzione progressiva prossima allo zero. In questa fase la diffusione del contagio potrà considerarsi in via di esaurimento.
Le ragioni di questo andamento possono essere dovute a due situazioni: o la diffusione del contagio nella popolazione progressivamente si satura fino a raggiungere il contagio collettivo (come succede ad esempio per Herpes virus) oppure i governi mettono in atto misure restrittive di contenimento finalizzate al raggiungimento della decrescita del contagio, come ha fatto inizialmente la Cina e come sta facendo l’Italia in questo momento.
Credo che non sia possibile prevedere la durata della pandemia almeno fino al raggiungimento della fase logistica. Una volta cominciato il rallentamento progressivo della crescita, come è avvenuto in Cina, sarà possibile capirne l’andamento futuro.
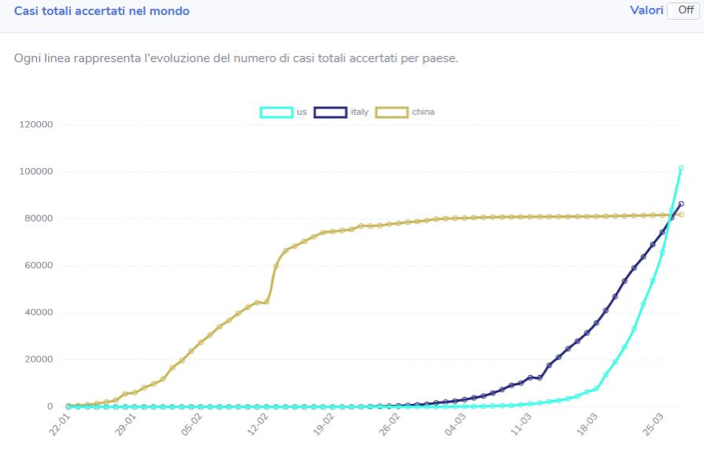 Per la Cina (colore marrone) si notino le fasi esponenziale e logistica. L’Italia (colore blu) e gli Stati Uniti (colore azzurro) si trovano ancora nella fase esponenziale.
Per la Cina (colore marrone) si notino le fasi esponenziale e logistica. L’Italia (colore blu) e gli Stati Uniti (colore azzurro) si trovano ancora nella fase esponenziale.
Fonte dati: Istituto Superiore di Sanità, Johns Hopkins University
Report: rainews24 http://www.rainews.it/ran24/speciali/2020/covid19/world.php
Il nuovo coronavirus SARS-CoV2 è stato definito non letale ma molto contagioso, che cosa significa?
Se parliamo di letalità (numero dei decessi/numero degli ammalati) il valore è decisamente basso, intorno al 5% (dato aggiornato al 03/04/2020). Le fasce maggiormente a rischio sono esattamente le stesse che potrebbero avere complicanze durante l’influenza stagionale: età avanzata, presenza di altre patologie, un fenomeno detto comorbidità, (obesità, diabete, malattie cardiache, malattie polmonari e renali)7.
L’elevata contagiosità in linea di massima è molto simile (ma sicuramente maggiore) dell’influenzavirus che conta ogni anno in Italia più di 7 milioni e mezzo di casi accertati. Tuttavia per il SARS-CoV-2 non è possibile stimarne la contagiosità con precisione a causa dell’errore che ci portiamo dietro fin dall’inizio dell’epidemia: lo screening parziale della popolazione non permette un quadro completo e realistico della diffusione del virus.
Le azioni di sorveglianza attiva con tamponi a tappeto e monitoraggio dei sintomi possono contribuire e in che modo ad affrontare l’emergenza?
Sicuramente in modo positivo. A livello epidemiologico avere il campionamento totale della popolazione permetterebbe di conoscere la reale distribuzione della malattia Covid-19, ma ragionevolmente è impossibile sottoporre a screening l’intera popolazione italiana (60 milioni di individui). In una crisi mondiale bisogna ottimizzare materie ed energie.
Personalmente procederei, nei limiti del possibile, con lo screening di tutte le persone che appartengono alle fasce maggiormente a rischio. Una sorveglianza attiva su queste persone, con eventuale monitoraggio dei sintomi in caso di positività, permetterebbe sicuramente di anticipare eventuali ricoveri mediante prevenzione della diffusione.
Una sorveglianza attiva sulle fasce a rischio permetterebbe di anticipare eventuali ricoveri @antonellopelosi
bit.ly/2X6Olopclicca per twittare
Per il resto della popolazione, anche se positiva ma asintomatica è sufficiente rispettare seriamente le norme restrittive messe in atto dal Governo riguardo la libera circolazione.
Rimanere a casa significa diminuire realmente le possibilità di contagio e per un patogeno nuovo come questo, contro il quale non abbiamo alcuna cura, attualmente rimane l’arma più efficiente.
Per quanto riguarda la malattia SARS non è mai stato trovato un vaccino. E’ possibile trovare un vaccino contro SARS-CoV2? Se sì, come funzionerebbe?
Non ci sono ad oggi vaccini contro SARS-CoV, SARS-CoV-2 e MERS-CoV.
Le cause sono molteplici; probabilmente da una parte c’è la natura altamente variabile dei coronavirus, soprattutto del gene S come detto prima. Poi c’è la distribuzione dei coronavirus; se osserviamo i 3 casi abbiamo a che fare con cifre totalmente diverse.
SARS-CoV: controllato in 6 mesi (da novembre 2002 a maggio 2003), con un bilancio di 800 decessi su 8000 casi distribuiti in 26 paesi globali.
MERS-CoV: ancora in corso con 912 decessi su 2494 casi distribuiti in 27 paesi globali. Attualmente i nuovi casi sono prevalentemente in Medio Oriente.
SARS-CoV-2: pandemia in corso con andamento crescente, distribuita globalmente tranne ai poli (in 181 paesi), con 53.975 decessi e 1.026.974 casi mondiali accertati (dato aggiornato al 03/04/2020).
Dunque prendere in considerazione gli sforzi per trovare un vaccino, in questo momento ha sicuramente una rilevanza maggiore. Le sperimentazioni di nuovi probabili vaccini a partire dagli anticorpi contenuti nel siero di persone guarite a Covid-19 sono incoraggianti anche se da verificare (immunizzazione passiva). Inoltre, sono in corso di sperimentazione anche una serie di terapie farmacologiche a base di antivirali (già presenti contro SARS, HIV, Ebola) o antimalarici (clorochina) che in qualche modo vanno a bloccare le fasi vitali del virus (ingresso, replicazione, assemblaggio); si tratta ad esempio di alcune varianti sintetiche di quei recettori cellulari menzionati all’inizio che legherebbero il virus impedendogli di legarsi alle cellule. Altre terapie, ad esempio a base di Tocilizumab (anticorpo monoclonale) mirano a bloccare la risposta immunitaria shock dell’organismo che porta alle complicazioni osservate: ARDS (Acute respiratory distress syndrome), sindrome da distress respiratorio acuto. Nei prossimi mesi con l’inizio delle sperimentazioni ci saranno sicuramente novità a riguardo.
Come facciamo a sapere che SARS-CoV2 ha un'origine animale e come avviene il passaggio da una specie all’altra fino all’uomo?
Un altro aspetto che accomuna SARS-CoV, MERS-CoV e SARS-CoV-2 riguarda i cosiddetti serbatoi naturali e gli ospiti occasionali8. Sappiamo che tutti i coronavirus di interesse umano utilizzano diverse specie di pipistrello (es. Rhinolophus affinis, Rhinolophus ferrumequinum) come serbatoio naturale. Sappiamo anche che, in linea di massima, prima di arrivare ad infettare l’uomo avviene il passaggio dal pipistrello ad un ospite intermedio: lo zibetto (Paradoxurus hermaphroditus) nel caso di SARS-CoV, il pangolino (Manis javanica) nel caso di SARS-CoV-2 e il dromedario (Camelus dromedarius) nel caso di MERS-CoV. Questo fatto è di notevole importanza per comprendere come e perché questi virus si diffondono nel regno animale. Il cosiddetto salto di specie (spillover) è stato valutato attraverso le comparazioni genetiche del nuovo coronavirus SARS-CoV-2 con la maggior parte dei coronavirus conosciuti presenti nella letteratura scientifica9, 10.
Dal confronto delle sequenze genetiche è emerso che:
- SARS-CoV-2 condivide il 96% dell’intero genoma con il coronavirus della specie di pipistrello Rhinolophus affinis (Bat Cov RaTG13) presente nella provincia di Yunnan (Cina);
- Il coronavirus trovato nel pangolino denominato Pangolin-CoV condivide il 91,02% dell’intero genoma con SARS-CoV-2;
- Il Pangolin-CoV condivide il 90% dell’intero genoma con il coronavirus del pipistrello Bat Cov RaTG13.
Queste sequenze genetiche di coronavirus vengono clusterizzate, ossia raggruppate insieme proprio sulla base della condivisione dell’intero materiale genetico. Dunque, se confrontiamo i genomi di SARS-CoV e SARS-CoV-2 vediamo quasi l’80% di similarità. MERS-CoV invece mostra una maggiore diversità rispetto ai primi due e questo viene descritto perfettamente mediante alberi filogenetici.
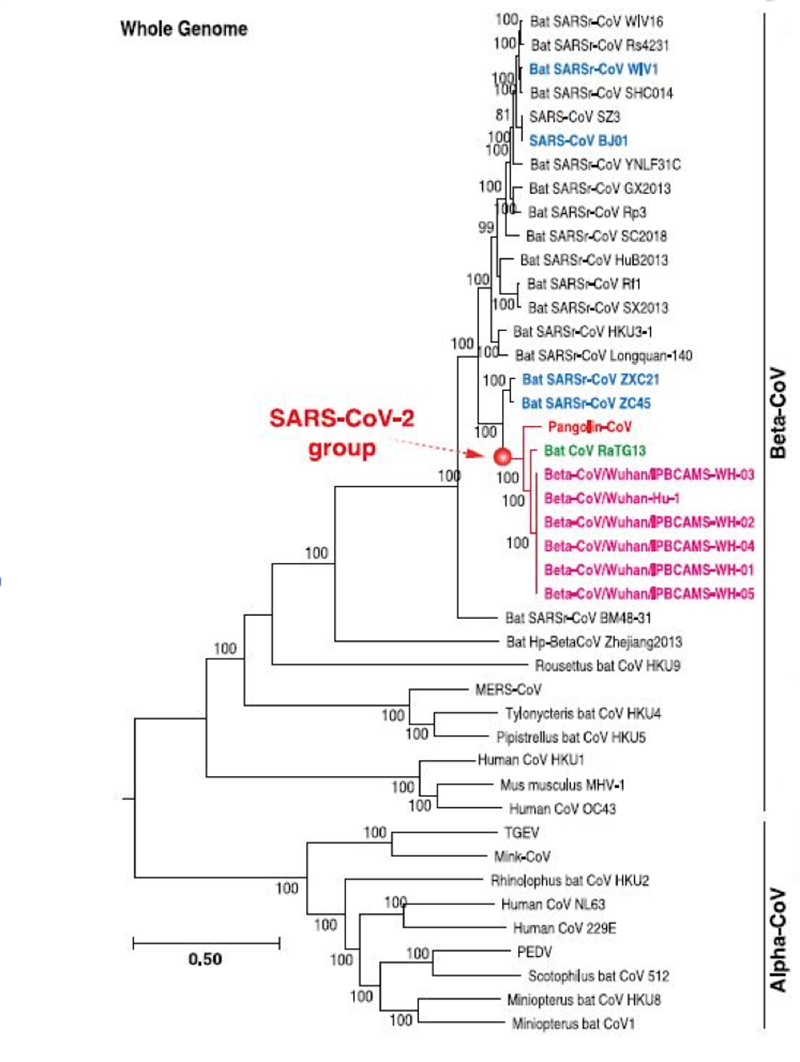
Si nota una vicinanza nell’albero filogenetico tra il Pangolin-Cov (in rosso), il Bat-Cov RaTG13 (in verde) e il gruppo dei coronavirus SARS-Cov-2 (in viola).
Inoltre, si nota come il coronavirus MERS-Cov si trova distante dal gruppo appena descritto a causa delle sue diversità genetiche, per questo definito outgroup rispetto al raggruppamento SARS-CoV like.
Il passaggio è avvenuto probabilmente a causa dell’uomo.
In Cina, sia il pangolino sia il pipistrello sono entrambe specie braccate per essere vendute nei mercati.
Le scaglie che ricoprono il corpo del pangolino, fatte di cheratina, vengono utilizzate nella medicina tradizionale cinese per curare alcune patologie (senza alcuna conferma dalla comunità scientifica dell’effettivo funzionamento).
Il bracconaggio di animali vivi ai fini commerciali, trasportati in condizioni “disumane” e macellati in spazi ristretti, con scarse norme igienico sanitarie per la vendita delle carni, favorisce sicuramente il contatto tra fluidi biologici (sangue, urina, feci) di specie animali diverse. Queste specie, serbatoi naturali di molti virus, si trovano artificialmente in contatto, mentre in natura sarebbero lontane tra loro, con nicchie ecologiche totalmente differenti. Tutto questo favorisce enormemente la trasmissione e il salto di specie di eventuali virus patogeni. Il caso del mercato del pesce di Whuan non è assolutamente il primo caso di “laboratorio biologico” per la nascita e la diffusione di nuovi patogeni. In Cina e in generale in estremo oriente sono documentate molte altre forme di diffusione simili avvenute in passato. SARS-CoV nel 2002 ad esempio si è diffuso nella provincia cinese del Guangdong con le medesime modalità.
Dato che molte epidemie si sono manifestate in seguito ad azioni antropiche che hanno favorito il contagio tra animali, potremo limitarne la diffusione in futuro grazie a comportamenti preventivi come la conservazione degli habitat e il rispetto di norme igienico-sanitarie?
Limitare lo sfruttamento delle risorse naturali mantenendo la conservazione degli habitat sicuramente permette di limitare il fenomeno dello spillover (salto di specie). Realisticamente fare questo in città estremamente affollate come Whuan (11 milioni di abitanti), nelle quali la richiesta di materie naturali è in crescita costante, risulta molto complicato. Ricordiamoci che ci sono molte città popolose come Whuan che soffrono il problema del sovraffollamento umano, per non parlare delle aree rurali praticamente fuori controllo. Inoltre, la deforestazione con la conseguente perdita di habitat costringe sempre più animali di specie diverse a contatti maggiori. Dunque i probabili “laboratori biologici” in realtà sono moltissimi. Sicuramente limitare il bracconaggio a livello capillare e il trasporto di animali vivi all’interno dei mercati, insieme al rispetto delle norme igienico sanitarie, garantirebbero una maggiore sicurezza nazionale e globale.
Qual è il ruolo della ricerca di base in una situazione di emergenza di salute pubblica come quella che stiamo vivendo?
La ricerca di base è la linfa vitale della ricerca applicata e andrebbe curata e privilegiata sempre, non solo nei momenti di emergenza. In questo caso in particolare, studiare la genetica dei patogeni (virus, batteri, funghi) permette di avere una base di partenza per eventuali emergenze sanitarie globali che potrebbero mettere a rischio l’intera popolazione umana.
La ricerca di base è la linfa vitale della ricerca applicata e andrebbe curata e privilegiata sempre @antonellopelosi
bit.ly/2X6Olopclicca per twittare

Coronavirus infografica © Carlo Taccari/BUONO
BIBLIOGRAFIA
1. Min J., Cella E., Ciccozzi M., Pelosi A., Salemi M., Prosperi M., (2016) The global spread of Middle East respiratory syndrome: an analysis fusing traditional epidemiological tracing and molecular phylodynamics. Global Health Research and Policy Sep 28;1:14. doi: 10.1186/s41256-016-0014-7.
2. Kumar S, Maurya VK, Prasad AK, Bhatt MLB, Saxena SK. Structural, glycosylation and antigenic variation between 2019 novel coronavirus (2019-nCoV) and SARS coronavirus (SARS-CoV). Virusdisease. 2020;31(1):13-21. doi: 10.1007/s13337-020-00571-5.
3. Zheng M, and Song L., Novel antibody epitopes dominate the antigenicity of spike glycoprotein in SARS-CoV-2 compared to SARS-CoV. Cell Mol Immunol, 2020 https://doi.org/10.1038/s41423-020-0385-z
4. Wan Y, Shang J, Graham R, Baric RS, Li F. Receptor Recognition by the Novel Coronavirus from Wuhan: an Analysis Based on Decade-Long Structural Studies of SARS Coronavirus. J Virol. 2020 17;94(7). pii: e00127-20. doi: 10.1128/JVI.00127-20.5. Huang C, Wang Y, Li X, Ren L, Zhao J, Hu Y, Zhang L, Fan G, Xu J, Gu X, Cheng Z, Yu T, Xia J, Wei Y, Wu W, Xie X, Yin W, Li H, Liu M, Xiao Y, Gao H, Guo L, Xie J, Wang G, Jiang R, Gao Z, Jin Q, Wang J, Cao B. Clinical features of patients infected with 2019 novel coronavirus in Wuhan, China. Lancet. 2020 15;395(10223):497-506. doi: 10.1016/S0140-6736(20)30183-5.
5. Willman M, Kobasa D, Kindrachuk J. A Comparative Analysis of Factors Influencing Two Outbreaks of Middle Eastern Respiratory Syndrome (MERS) in Saudi Arabia and South Korea. Viruses. 2019 3;11(12). pii: E1119. doi: 10.3390/v11121119.
6. Song Z, Xu Y, Bao L, Zhang L, Yu P, Qu Y, Zhu H, Zhao W, Han Y, Qin C. From SARS to MERS, Thrusting Coronaviruses into the Spotlight. Viruses. 2019 14;11(1). pii: E59. doi: 10.3390/v11010059.
7. Huang C, Wang Y, Li X, Ren L, Zhao J, Hu Y, Zhang L, Fan G, Xu J, Gu X, Cheng Z, Yu T, Xia J, Wei Y, Wu W, Xie X, Yin W, Li H, Liu M, Xiao Y, Gao H, Guo L, Xie J, Wang G, Jiang R, Gao Z, Jin Q, Wang J, Cao B. Clinical features of patients infected with 2019 novel coronavirus in Wuhan, China. Lancet. 2020 15;395(10223):497-506. doi: 10.1016/S0140-6736(20)30183-5.
8. Tilocca B, Soggiu A, Musella V, Britti D, Sanguinetti M, Urbani A, Roncada P. Molecular basis of COVID-19 relationships in different species: a one health perspective. Microbes Infect. 2020 17. pii: S1286-4579(20)30048-4. doi: 10.1016/j.micinf.2020.03.002.
9. Andersen K G, Rambaut A, Lipkin W I, Holmes E C, Garry R F. The proximal origin of SARS-CoV-2. Nature Medicine, 2020. https://doi.org/10.1038/s41591-020-0820-9
10. Zhang T, Wu Q, Zhang Z. Probable Pangolin Origin of SARS-CoV-2 Associated with the COVID-19 Outbreak. Curr Biol. 2020 Mar 19. pii: S0960-9822(20)30360-2. doi: 10.1016/j.cub.2020.03.022.












